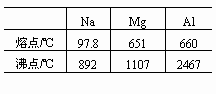
碱金属一般熔点较低,随原子序数增加熔沸点降低与水反应时,由于熔点低,碱金属大多会熔化成小球碱金属的熔点沸点随原子序数增加而降低,因而碱土金属的熔点沸点也会具有这变化规律碱金属单质的标准电极电势很小,具有很强的反应活性,能直接与很多非金属元素形成离子化合物,与水反应生成氢气,能;碱金属的密度变化规律碱金属的密度变化规律是随核电荷数的增大而增大,从上往下金属性增强,单质还原性增强,熔沸点降低,密度增大元素金属性强的的单质还原性强,阳离子氧化性弱,元素非金属性强的则相反钾的密度比钠的密度小对钾来说,核对最外层引力较小,体积增大的效应大于相对原子质量增加。
随着原子序数的增加,熔沸点降低随着原子半径增大,熔沸点降低;随着原子序数的增加,碱金属的熔沸点变化规律表现出随着原子半径的增大而降低这是因为碱金属原子随着原子序数的增加,原子半径增大,金属键减弱金属键的强度与金属离子的半径和电荷有关,原子半径增大意味着金属离子间的距离增加,从而金属键的引力减弱,导致熔沸点降低。
1 碱金属一族的熔沸点在这一列元素中随原子序数的增加而降低2 这可以通过元素周期表的排列规律得到解释,因为在这一族元素中,原子结构中的最外层电子数相等,核电荷数逐渐增加,原子半径逐渐缩小,电子云被吸得更紧,因此元素的电负性逐渐增强,金属元素的性质变得更加活泼,相似价电子云层向外扩张;碱金属单质的原子以金属键作用,原子序数增大时,原子半径增大,金属键的键长变大,破坏金属键所需的能量减小,所以熔沸点依次降低非金属单质是以分子形态出现的,相互间的作用力为范德华力就是分子间的作用力,原子序数增大时,分子量也增大,分子间的作用力就增大,所以熔沸点逐渐升高。
碱金属不都是金属嘛,所以熔沸点是由金属键键能决定,在所带电荷相同的情况下,原子半径越小,金属键键能越大抓得紧的感觉,所以碱金属的熔沸点递变规律是从上到下熔沸点依次降低;2同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增第一主族的碱金属熔沸点是由金属键键能决定,在所带电荷相同的情况下,原子半径越小,金属键键能越大,所以碱金属的熔沸点递变规律是从上到下熔沸点依次降低第七主族的卤素,其单质是分子晶体,故熔沸点由分子间。
所以 第一主族的碱金属熔沸点是由金属键键能决定,在所带电荷相同的情况下,原子半径越小,金属键键能越大,所以碱金属的熔沸点递变规律是从上到下熔沸点依次降低 第七主族的卤素,其单质是分子晶体,故熔沸点由分子间作用力决定,在分子构成相似的情况下,相对分子质量越大,分子间作用力也越大;1 碱金属的熔沸点呈现一个明显的下降趋势,随着原子序数的增加而降低2 原子序数的增加带来原子半径的增大,这直接影响了金属键的强度3 金属键的强度是决定金属熔沸点的重要因素,强度减弱导致熔沸点降低4 从锂Li到铯Cs,碱金属的熔沸点依次降低,这一变化规律反映了原子序数与熔沸。
碱金属的密度随着原子序数的增加总体上呈现增大的趋势然而,在从钠到钾的过程中,出现了密度反常的现象这是因为虽然相对原子质量的增加会导致密度的增大,但原子体积的增大对密度的贡献更大,导致钾的密度反而小于钠2 碱金属的熔沸点递变规律 碱金属的熔点和沸点随着原子序数的增加逐渐降低这一。

碱金属的熔沸点变化规律为什么
所以在固体中原子间相互作用较弱,金属键很容易断裂,所以碱金属的熔点和沸点都较低又金属的熔沸点主要取决于其中的金属键强度金属阳离子的电荷越高,半径越小,则金属键的强度越大LI,Na,K,Rb,Cs为同主族元素,原子半径依次增大,电荷相同因此,随着半径的增大,金属键依次减弱,所以熔沸点逐渐降低。
金属键的强度随着原子半径增大而减弱,所以熔点降低。
是对的啊,我最近正在看碱金属方面的内容,随着核电荷数的增加,其密度逐渐增大,熔沸点,硬度都减小,这是因为随核电荷数增大,其阳离子半径越来越大,与自由电子的作用力越来越弱为什么与非金属单质不一样是因为他们的单质形成的键是不同的键,如有分子晶体,原子晶体等,影响他们熔沸点的因素就会不。
碱金属熔点沸点为什么逐渐升高
1、碱金属的熔沸点变化规律是随着原子序数的增加而降低随着原子序数的增大,碱金属原子的半径也随之增大,导致金属键的强度减弱金属键的强度是影响金属熔沸点的关键因素之一,当金属键强度减弱时,金属的熔沸点就会降低从锂Li到铯Cs,碱金属的熔沸点依次降低。
2、碱金属属于金属晶体,从金属键的角度考虑从上往下,金属阳离子半径增大,对外层电子束缚能力减弱,金属键减弱熔沸点降低 卤素属于分子晶体,考虑范德华力 从上往下,分子的相对分子质量增大,范德华力增强,熔沸点升高。
3、碱金属元素从上到下递变规律如下碱金属元素,金属性从上到下依次增加,单质还原性依次增强,单质与O2反应的产物越来越复杂,反应程度越来越剧烈,碱金属元素,从上到下,单质的密度逐渐增大,钾反常,金属键从上到下依次减弱,所以熔沸点逐渐降低。







添加新评论